近日,动物科技学院“肌肉生物学与生猪遗传改良创新团队”吴江维教授联合多家单位在Cell Metabolism期刊发表题为“GDF15 is a major determinant of ketogenic diet-induced weight loss”的研究论文,并被选为该期的亮点文章。该项研究利用三种物种及六种基因编辑动物模型,系统揭示了生长分化因子GDF15在生酮饮食发挥体重管理中不可或缺的作用机制。

以高脂肪、低碳水化合物为主要组分的生酮饮食近年来受到广泛关注。生酮饮食增加机体血液中酮体水平,这种“代谢酮症”状态模拟了禁食状态,机体的两大器官心脏和大脑可以利用酮体替代葡萄糖作为其能量来源。基于生酮饮食模拟饥饿的特点,在当前肥胖全球化背景下,生酮饮食在体重管理中的有益作用引起了大家的广泛关注与热烈追捧,但其潜在的作用机制仍不清楚。生长分化因子15(Growth differentiation factor 15,GDF15)属于转化生长因子TGF-β超家族中的成员,首次发现于1997年。近年来包括该团队在内的多个研究小组发现GDF15具有显著抑制食欲的生理学功能,因而在体重管理中发挥着重要作用。与此巧合的是,多项文献报道和临床研究表明,生酮饮食亦能显著降低机体的食物/能量摄入,那么生酮饮食与GDF15 在体重管理中是否存在着某种潜在的关联呢?
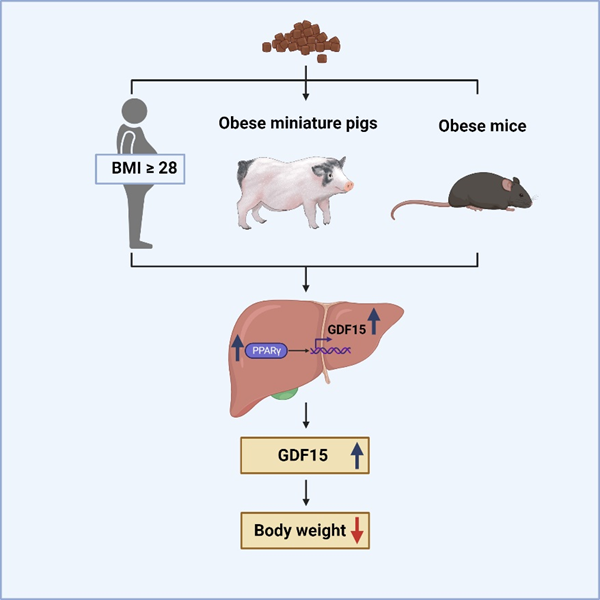
研究图文摘要
本研究聚焦生酮饮食显著降低机体的食物(能量)摄入背后的机制这一科学问题,研究人员首先以小鼠为研究对象,发现生酮饮食的小鼠在体重下降的同时,血液GDF15水平显著升高。当给予小鼠其他几种广泛使用的体重管理饮食(包括地中海饮食 、低脂肪饮食、高蛋白饮食、低血糖指数饮食)和两种禁食方式(隔日禁食和限时进食),均未观察到GDF15水平升高的现象,表明生酮饮食能特异性引起GDF15水平升高。该团队进一步以小型猪为模型,通过生酮饮食饲喂,观察到了类似于小鼠的结果,实验动物也表现出体重下降与GDF15水平升高的规律。最后通过生酮饮食肥胖人群的试验,发现生酮饮食可普遍降低体重并升高血液GDF15水平。
为探究GDF15在生酮饮食的体重管理中是否发挥着必需的作用,研究人员使用了GDF15及其受体GFRAL全身性敲除小鼠模型。他们发现无论敲除GDF15本身或其受体GFRAL,生酮饮食降低体重的作用均被大幅削弱,这一现象也在GDF15中和抗体实验中得到证实,表明GDF15 对于生酮饮食介导的小鼠体重管理是不可或缺的。
随后,研究人员重点关注生酮饮食如何诱导GDF15的升高。他们发现生酮饮食显著增加小鼠及小型猪肝脏中GDF15的表达。该发现在构建的肝脏特异性GDF15敲低小鼠模型中得到证实,明确肝脏是生酮饮食中GDF15增加的主要来源。通过RNA-Seq测序,研究人员发现生酮饮食条件下,肝脏的PPAR信号通路,尤其是PPARγ及其靶标在内的靶基因显著上调,提示肝脏PPARγ 和GDF15 之间可能存在相关性。他们通过体外和体内试验证实了肝细胞PPARγ能够直接调控GDF15的转录和表达。有趣的是,尽管转录因子PPARγ在脂肪细胞中高表达,研究人员发现PPARγ不能调控脂肪细胞中GDF15的转录与分泌。以上结果表明PPARγ 对GDF15 的转录调控作用在物种间高度保守但具有明显的细胞特异性。
最后,为在活体水平阐明生酮饮食条件下肝脏组织PPARγ与GDF15 之间的关系,研究人员分别使用了腺相关病毒介导的肝脏PPARγ敲低模型和肝细胞特异性PPARγ敲除小鼠模型,发现肝脏 Pparγ 敲低/敲除后,GDF15水平下降,生酮饮食的体重控制效果显著减弱。同时,通过构建GDF15肝脏过表达模型和全身性注射重组GDF15蛋白的小鼠模型,证实了肝脏Gdf15表达减少和循环GDF15水平降低是生酮饮食有益作用在肝脏PPARγ敲除小鼠消除的主要原因。
该项研究首次系统揭示了GDF15在生酮饮食发挥体重管理中不可或缺的作用机制,增进了对生酮饮食发挥代谢调控作用的理解。本研究是“一猪两用”领域的又一次探索尝试,发现的生酮饮食调控机体循环GDF15水平进而调控动物能量摄入的信号通路,对动物脂质沉积的精准营养调控具有重要的指导意义。

受邀创作杂志封面 (创作灵感:封面以被誉为“世界第八大奇迹”的兵马俑为主体,描绘了一幅西北地区将士热烈集会的场景,兵马俑将军发现以牛油果为代表的生酮饮食能够显著升高机体GDF15水平,他兴奋的号召士兵们跟随他的脚步,深入探究GDF15的分泌和产生)
我校为本研究第一单位,动科学院博士研究生卢军锋、已毕业硕士朱梦清、夏博副教授及西京医院内分泌科张娜娜医生为本文的共同第一作者,动科学院吴江维教授、西京医院内分泌科李晓苗主任为本文共同通讯作者。国家食品安全风险评估中心杨辉副研究员、空军军医大学张英起教授对本研究做出了重要贡献。剑桥大学Sir Stephen O’Rahilly及David B. Savage教授、加拿大麦克马斯特大学 Gregory R. Steinberg教授等对本研究提出了宝贵的建议与意见。本研究得到国家重点研发计划、国家自然科学基金、陕西省创新人才推进计划等项目资助。团队带头人杨公社教授为该项目的顺利实施提供团队支撑和资金支持。
原文链接:https://www.sciencedirect.com/science/article/pii/S155041312300414X
编辑:张晴
终审:徐海