近日,化学与药学院裴志超教授团队在分子间二硫键引导的超双亲纳米药物递送体系研究领域取得新进展,研究成果以“A disulfide-induced supra-amphiphilic co-assembly for glycosylated pro-drug-photosensitizer nanoparticles in combination therapies”为题发表于国际著名化学期刊《Chemical Communications》。博士研究生靳文娟为论文的第一作者,裴志超教授为通讯作者。
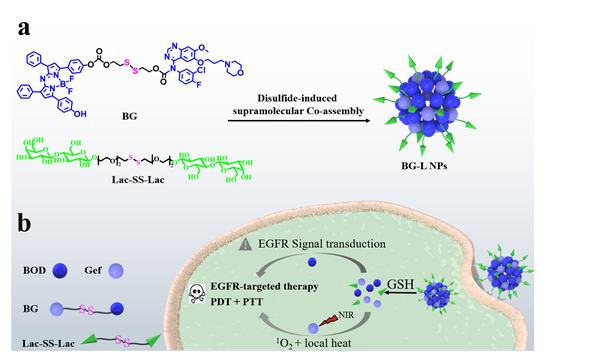
在抗肿瘤治疗中,常用具有还原型谷胱甘肽(GSH)响应性的二硫键修饰抗肿瘤药物,合成肿瘤微环境响应性释放的前药分子以降低药物的毒副作用,但由于大部分的抗肿瘤药物的疏水性,这类前药分子存在生物相容性差,药物递送效率低的问题。为解决这一科学问题,疏水前药分子的多种亲水/靶向基团的共价/非共价修饰被广泛研究。该团队首先合成了含二硫键的靶向亲水分子—二硫二聚乳糖(Lac-SS-Lac),然后以二硫键引导的分子间的S…S键相互作用和含二硫键的疏水的前药-光敏剂分子(BG),通过超分子共组装的方式构建了靶向超双亲纳米药物递送体系(BG-L NPs)。该体系避免了复杂两亲分子的合成,不仅制备简单,且具有多功能性(良好的生物相容性、稳定性、高载药量、低药物泄漏、靶向可控释放),实现了疏水药物吉非替尼(Gef)和光敏剂(BOD)的高效率靶向共递送和化疗和光疗联合抗肿瘤效果。
这项工作为首次以分子间硫键为引导构建了超双亲纳米体系,为疏水性药物的高效率靶向共递送提供了一种新的简单且具有通用性的亲疏水超分子共组装策略,为非共价键硫键在超双亲纳米药物递送体系方面的应用提供了新平台。
该研究得到了国家自然科学基金面上项目(22171230和21877088)和陕西省社会发展科学技术项目(2021SF-120)的资助。
原文链接:https://pubs.rsc.org/en/content/articlelanding/2022/cc/d2cc04777b
编辑:张晴
终审:徐海