近日,化药学院裴志超教授团队在基于金属配位超分子自组装策略的糖靶向纳米药物研究领域取得新进展,研究成果以“A glycol nanomedicine via a metal-coordination supramolecular self-assembly strategy for drug release monitoring and chemo-chemodynamic therapy”为题,发表在Chemical Communications上。硕士研究生李佳慧与博士研究生王毅为论文共同第一作者,裴玉新教授为通讯作者。
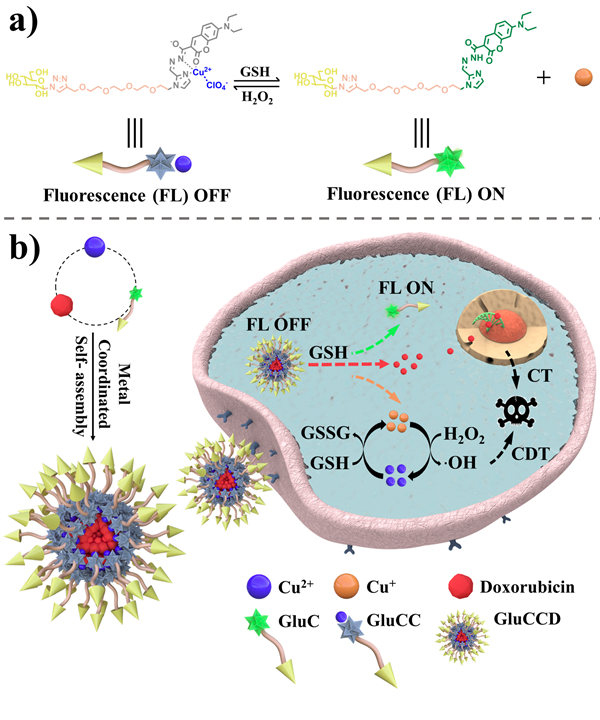
在肿瘤的化学治疗(CT)中,化疗药物对正常细胞的毒副作用大,且单一化学疗法抗肿瘤效果差。化疗药物释放监测在肿瘤治疗中起着至关重要的作用,但是化疗药物通常荧光微弱甚至无荧光,并且其结构修饰困难,还可能影响药物疗效。为解决这些问题,该团队构建了一种基于金属配位超分子自组装策略的糖靶向纳米药物以实现化学和化学动力学疗法的联合治疗。该团队首次合理设计合成了一种葡萄糖修饰的香豆素衍生物GluC,作为药物释放监测剂。铜离子可以将GluC与疏水化疗药物阿霉素(DOX)连接,用于猝灭GluC的荧光,并作为类芬顿反应的催化剂。由于Warburg效应和肿瘤细胞微环境中过量表达的谷胱甘肽(GSH),纳米药物可以靶向癌细胞并在癌细胞内降解,被释放的DOX和类芬顿反应产生的羟基自由基(·OH)可以发挥有效的杀伤癌细胞的作用。此外,GluC恢复的强荧光信号可以有效监测释放的DOX。本研究提供了一种新的基于金属配位超分子自组装策略的纳米药物,用于癌症靶向、自我监测和联合治疗。
该研究得到国家、陕西省和学校有关等项目资助。
链接原文:https://pubs.rsc.org/en/content/articlelanding/2022/cc/d2cc00159d
编辑:王学锋
终审:徐海