近日,化学与药学院天然产物化学生物学及高值利用高锦明团队在《Science Advances》上发表题为“Isothiocyanate-mediated cyclization of phage-displayed peptides enables discovery of macrocyclic binders的论文”。该研究突破性发现:利用一种结构简单的异硫氰酸酯衍生物交联剂,成功开发出一种pH值调控的“智能锁扣”式环化新策略。化学与药学院2022级博士研究生白利文和中南民族大学硕士研究生淡婷为本文共同第一作者,高锦明教授以及兰州大学天然产物化学全国重点实验室雷新响教授为本文共同通讯作者。
当前,大环肽已发展成为分子识别工具与先导化合物发掘的重要研究方向。此类分子兼具小分子与生物大分子的特性,形成了独特的生物学优势:一方面保留较好的膜通透潜力,另一方面在靶向传统难以干预的蛋白质靶点(如蛋白质-蛋白质相互作用界面)方面展现出显著潜力。噬菌体展示技术是筛选高亲和力肽配体的强大工具,但其应用的核心挑战在于如何在噬菌体表面实现高效、特异且无损活性的肽链环化。此外,有限的可修饰位点也制约了成环骨架的多样性。因此,发展一种条件温和、精准可控、并能引入优势药效骨架的新颖环化平台,是推动环肽药物发现的关键。
该研究策略可在生理缓冲条件下,通过一步反应于噬菌体表面高效构建结构稳定、包含硫脲药效团的大环肽库。通过精确调节反应环境的pH,可实现“N端-侧链”与“侧链-侧链”两种环化模式之间实现可控切换,从而显著拓展环肽骨架的结构多样性与构象空间。基于该平台,研究团队成功面向亲环蛋白D(Cyp D)、Kelch样ECH关联蛋白1(Keap1)及双微体同源蛋白2(MDM2)等多个关键疾病靶点开展筛选,获得了一系列具有亲和力高、活性达纳摩尔至微摩尔级水平的环肽抑制剂,充分体现了该平台在先导化合物发现与创新药物研究中的应用潜力。(图1)。
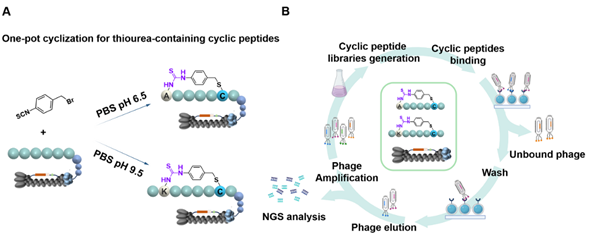
图1. pH调控的异硫氰酸酯策略用于构建噬菌体展示硫脲环肽库
研究首先在模型肽层面系统验证了该策略的化学选择性与pH依赖的反应机理。在弱酸性缓冲液(pH 6.5)中,异硫氰酸酯基团优先、选择性地与肽链N末端α-氨基反应,从而专一实现“头-侧链”环化;而在碱性条件(pH 9.5)下,反应则转而与赖氨酸残基的ε-氨基高效偶联,完成“侧链-侧链”环化。两种路径均能以高收率生成含有稳定硫脲基团的环肽产物。随后,研究团队在噬菌体pIII融合蛋白及完整病毒颗粒水平对该反应体系进行了全面验证:质谱分析确证了环化产物的精确结构;Pull-down实验表明环化修饰效率显著;更为关键的是,噬菌体滴度实验显示,在优化条件下该化学修饰对噬菌体的感染活性无明显影响,能够充分满足后续大规模功能性筛选对载体完整性的要求(图2)。为了进一步确保环化反应的高度位点特异性,避免对噬菌体自身蛋白的非预期修饰,作者构建了展示外源线肽和TEV酶切位点的噬菌体突变体,并对蛋白酶消化后释放的环化产物进行质谱鉴定。结果在分子层面直接证明,该策略具备良好的生物正交性与位点专一性。
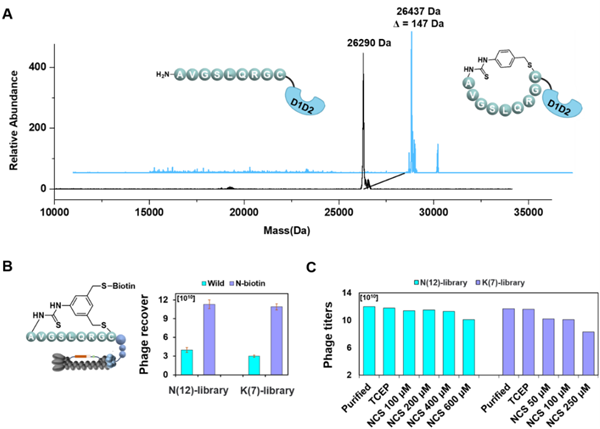
图2. 环化策略在噬菌体平台上的高效性与生物相容性验证
基于该稳定可靠的平台,研究团队进一步构建了两种硫脲类环肽库:在pH 6.5下环化的“N(12)库”与在pH 9.5下环化的“K(7)库”。针对线粒体关键调控蛋白Cyp D,从“N(12)库”中成功筛选出环肽抑制剂CD1,其半抑制浓度(IC₅₀)为4.14 µM,且其结合亲和力较线性前体提升逾30倍,充分表明环化策略与硫脲骨架能够有效限制构象自由度、稳定活性构象,从而显著增强分子识别与功能活性(图3)。
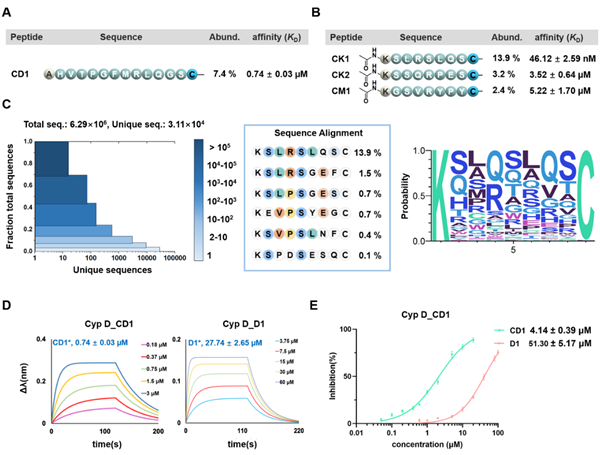
图3. 基于该平台发现的硫脲类环肽配体。
尤为值得关注的是,研究团队从“K(7)库”中获得了靶向Keap1蛋白的高活性环肽CK1,其解离常数达到46nM,并可通过效竞争性结合有效阻断Keap1/Nrf2这一重要的蛋白质-蛋白质相互作用。此外,针对肿瘤靶点MDM2亦成功筛选得到具有明确结合活性的环肽配体(图4)。上述结果从多个靶点与作用模式层面系统证明,该平台在面向不同作用机制靶点的活性环肽发现方面具备良好的通用性、筛选效率与应用拓展潜力。
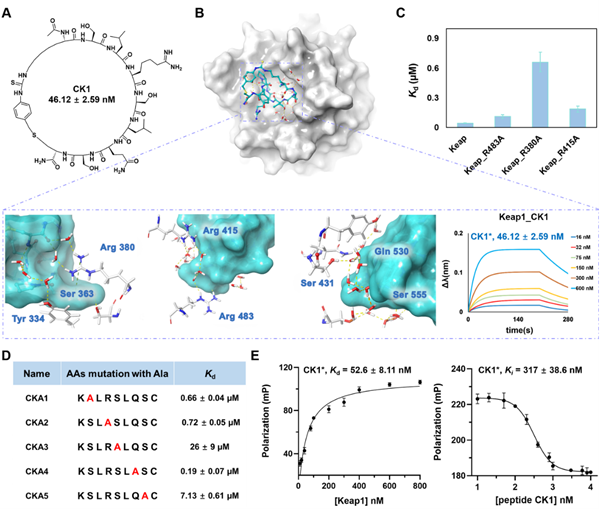
图4. 硫脲类环肽配体 与 Keap1 或 Keap1 突变体的亲和鉴定。
综上,本工作不仅为环肽药物的研发提供了一个极具潜力的工具,也为发展化学驱动的新一代噬菌体展示技术提供了创新性的研究思路。
该研究得到国家自然科学基金和甘肃省科技项目资助。
编辑:王学锋
终审:刘玉峰